Filmwaage
Grundlagen
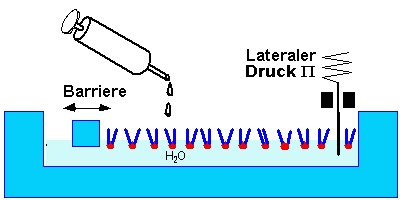
Die Eigenschaften von dünnen, an die Wasseroberfläche gebundenen Filmen aus amphiphilen Molekülen läßt sich mit einer sogenannten Filmwaage untersuchen. Diese besteht aus einem wassergefülltem Teflontrog, in dem eine bewegliche Barriere die Wasseroberfläche auf einer Seite dicht abschließt.
Eine bekannte Menge amphiphiler Moleküle [1] wird in einem spreitendem Lösungsmittel [2] aufgelöst und einige ul der Lösung mit einer Mikrospritze auf die Subphase aufgetropft. Das Lösungsmittel verdampft und eine definierte Anzahl Moleküle bleibt auf der Oberfläche zurück. Dadurch wird eine bestimmte Fläche pro Molekül eingestellt, die durch Bewegen der Barriere verändert werden kann.
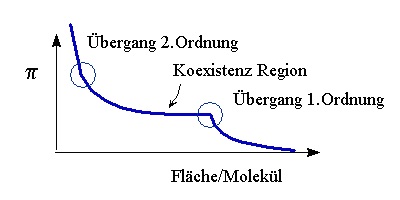
Phasenänderungen des Systems, z.B. der Kettenordnungsübergang bei Lipiden, erscheinen in der Isotherme als Bereiche konstanten Druckes - ein Phasenübergang erster Ordnung mit Koexistenz von zwei Phasen - oder als Knick in der Isothermen - ein Phasenübergang zweiter Ordnung. Die Messung von Isothermen ist deswegen grundlegend zur Charakterisierung der Systeme. Darauf aufbauend kommen dann andere Methoden zum Einsatz.
Außer der Fläche pro Molekül lassen sich bei Filmwaagenexperimenten die Temperatur, die Subphase (Salzgehalt, pH-Wert, Lösungen von Polyelektrolyten oder Proteinen) und die Atmosphäre (Luft, flüchtige Organische Substanzen) ändern.
Die einfachste Messgröße ist die Oberflächenspannung [3] g. Diese ist proportional zur Kraft mit der ein Filterpapierstückchen in das Wasser gezogen wird. Für eine reine Wasseroberfläche bei Raumtemperatur ist gWater=72.4mN/m. Die oberflächenaktiven Moleküle verringern die Oberflächenspannung. Die Differenz P=gWater-g wird lateraler Druck genannt. Die Repulsion der amphiphilen Moleküle führt mit abnehmender Fläche zu Abnahme der Oberflächenspannung, d.h. zu einer Zunahme des Lateralen Druckes - ganz analog zum dreidimensionalen System. Entsprechen misst man zur theromdynamischen Charakterisierung Isothermen im Druck-Flächen-Diagramm.
Praxis
Weil Oberflächenexperimente schon durch kleine Konzentrationen von Fremdstoffen gestört werden können, bedeuten Filmwaagenexperimente vor allen Dingen: Putzen. Mehrfaches Füllen und Absaugen mit hochreinem Wasser nach Reinigen mit Tensid- oder Propanollösungen, oder Auswischen mit Lösungsmitteln nimmt die meiste Zeit in Anspruch. Das Messen der Isothermen selbst erfolgt dagegen weitgehend computerkontrolliert.
Anmerkungen
[1] Amphiphile Moleküle bestehen aus wasserliebenden, also polaren oder ionischen, und wasserabstoßenden, unpolaren molekularen Gruppen. Ein einfaches Beispiel sind Fettsäuren. Für Filmwaagenexperimente müssen die Moleküle zumindest metastabil an die Oberfläche gebunden sein, sie müssen also eine geringe Wasserlöslichkeit besitzen. Das erreicht man durch einen genügend großen hydrophoben Molekülteil.
[2] Ein Lösungsmittel spreitet (spreiten von englisch to spread), wenn die Oberflächenenergie Wasser-Luft größer ist als die Oberflächenenergien Lösungsmittel-Wasser und Lösungsmittel-Luft zusammen. Dann ist das Ausbilden eines dünnen Filmes energetisch vorteilhaft. Mit diesem Film werden auch die gelösten Amphiphile auf der Oberfläche verteilt. Ein typische Lösungsmittel ist Chloroform oder Mischungen aus überwiegend Chloroform mit polaren Molekülen (Ethanol, Methanol). Das Chloroform sorgt für das Spreiten, die polaren Beimischungen erhöhen die Löslichkeit der Amphiphile.
[3] In den Anfängen der Filmwaagenexperimente wurde die Oberfächenspannung über die Kraftwirkung auf ein bewegliche Barriere mit einer Waage bestimmt - daher der Name Filmwaage.
